Réplication autonome dans l'eccDNA : preuves, questions ouvertes et comment le séquençage peut aider

Les ADN circulaires extrachromosomiques (eccADN) sont-ils simplement des débris passifs issus de l'instabilité génomique, ou certains d'entre eux se répliquent-ils de manière autonome et persistent-ils en tant qu'épisomes véritables ? Ce guide adopte une position claire et argumentée : il existe des preuves solides et émergentes que, du moins un sous-ensemble d'eccADN, peut soutenir des comportements similaires à la réplication, et le domaine dispose désormais des outils nécessaires pour obtenir des preuves décisives dans les cellules humaines. Nous exposons également les lacunes et les expériences précises qui peuvent les combler.
Tout au long de ce texte, nous distinguons les petits eccDNA (souvent appelés microDNA ; généralement <10 kb) des grands amplificateurs circulaires associés au cancer (ecDNA ; de dizaines de kilobases à des mégabases). Notre attention se porte sur les petits eccDNA et la question de la réplication autonome dans les eccDNA en tant que mécanisme de persistance et d'impact fonctionnel. Nous ancrons l'argument dans la biologie de la réplication, les démonstrations inter-systèmes de l'activité d'origine, et les flux de travail basés sur le séquençage qui peuvent vérifier ou falsifier la réplication autonome avec des preuves orthogonales.
Qu'est-ce qui compte comme réplication autonome dans l'eccDNA ?
Par réplication autonome dans l'eccDNA, nous entendons le maintien post-formation où une molécule d'ADN circulaire initie la réplication de l'ADN à partir de sa propre séquence semblable à un origine et soutient la progression de la fourche indépendamment de son locus chromosomique. Cela se distingue de la biogenèse dépendante de la réplication (par exemple, lorsque le stress de réplication aide à créer de l'eccDNA via une réplication induite par rupture) et de l'amplification en cercle roulant in vitro. Les preuves de la réplication autonome devraient démontrer :
- Origine de la fusion sur le cercle (ou recrutement de facteurs d'origine aux séquences circulaires) dans des conditions normales de cycle cellulaire.
- Intermédiaires de réplication caractéristiques des modèles circulaires (arcs en bulle/structures thêta) dans l'ADN cellulaire.
- Incorporation des étiquettes de réplication (BrdU/EdU) dans la fraction circulaire, au-dessus du fond apparié.
- Confirmation de séquençage orthogonal que les molécules étiquetées ou structurées sont de véritables cercles avec des jonctions définies.
Ces critères vont collectivement au-delà de "les cercles existent" à "les cercles se répliquent." Ils sont délibérément conservateurs pour éviter de confondre les corrélats de la biogenèse avec le maintien.
Les preuves que nous avons jusqu'à présent (cellules humaines et indices inter-systèmes)
Un ensemble croissant d'observations soutient la plausibilité de la réplication autonome dans l'eccDNA, même si les preuves revues par des pairs concernant les petits cercles dans les cellules humaines restent limitées.
La biogenèse des cellules humaines est associée à la réplication. En 2024, Gadgil et ses collègues ont montré que des microsatellites ectopiques, formant de l'ADN non-B, intégrés dans des cellules humaines génèrent des eccDNAs par des mécanismes dépendants de la réplication, compatibles avec la réplication induite par rupture et le changement de modèle. La mutagenèse s'est étendue sur plusieurs kilobases, et les agents de stress de réplication ont modifié les profils d'eccDNA. Ces découvertes rendent difficile l'argument selon lequel la réplication est sans rapport avec la biologie des eccDNA, même si elles ne prouvent pas encore que les cercles, une fois formés, continuent à se répliquer d'eux-mêmes. Voir la démonstration détaillée dans l'étude NAR Cancer de Gadgil et al. (2024), qui fournit de solides preuves de biogenèse liée à la réplication et une base méthodologique pour des tests axés sur l'origine dans les systèmes humains.
Démonstrations inter-systèmes des origines fonctionnelles sur des réplicons de type eccDNA. En dehors des petits eccDNA humains, il existe des preuves fonctionnelles directes que les séquences portées par des cercles peuvent agir comme des origines. Chez les plantes, des segments de type origine provenant du réplicon eccDNA d'Amaranthus palmeri ont permis une réplication autonome dans la levure lorsqu'ils ont été clonés dans des vecteurs sans ARS. Cette étude de Molin et al. (2020) a validé que certains réplicons extrachromosomiques portent de véritables séquences de réplication autonome (ARS) avec les caractéristiques de séquence attendues (richesse en AT, éléments de déroulement de l'ADN). Dans la levure elle-même, une fraction substantielle des eccDNA abrite des motifs ARS/ACS et peut se répliquer et se propager sous sélection. Ensemble, ces données prouvent le principe : si un eccDNA contient une origine qui est compétente dans un système de réplication eucaryote, la réplication autonome est possible.
L'ecDNA humain dans le cancer comme comparateur conceptuel. Bien que notre attention soit portée sur le petit eccDNA, le grand ecDNA dans les cellules cancéreuses humaines engage clairement la machinerie de réplication. Les études sur l'ecDNA montrent des origines redistribuées et des fourches vulnérables sous stress, soulignant que l'ADN circulaire peut être un substrat pour l'initiation de la réplication et le mouvement de la fourche dans les cellules humaines. La topologie et la taille sont différentes, mais le message mécaniste est pertinent : les modèles circulaires ne sont pas invisibles au programme de réplication.
Où se situe "eccDNA Michael Leffak". Michael Leffak et ses collègues ont longtemps fait progresser l'étude des origines de réplication dans les chromosomes des mammifères, en particulier les caractéristiques de séquence et de chromatine qui favorisent l'initiation. Bien que nous n'ayons pas trouvé d'articles évalués par des pairs sur des cellules humaines qui démontrent explicitement "eccdna michael leffak replication" pour de petits cercles, ce corpus de biologie des origines informe exactement comment tester les eccDNAs pour leur capacité d'initiation : enrichir les séquences riches en AT/DUE, cartographier la liaison ORC/MCM et mesurer le signal de brin naissant. En d'autres termes, le cadre des origines de réplication attribué au domaine de Leffak offre la logique et les tests nécessaires pour traiter la question de la réplication autonome dans les eccDNA sans exagérer.
Le constat final sur les preuves. La combinaison de (1) la biogenèse dépendante de la réplication dans les cellules humaines, (2) l'activité d'origine fonctionnelle sur les réplicons d'eccDNA à travers les systèmes, et (3) la réplication claire de grands ADN circulaires dans les cellules cancéreuses humaines constitue un soutien fort et convergent indiquant que certains petits eccDNAs pourraient se répliquer de manière autonome. Ce qui manque, c'est une démonstration décisive, à travers plusieurs tests, dans les cellules humaines qui relie l'occupation de l'origine, le marquage de la réplication et la structure circulaire aux mêmes molécules. C'est ce que les sections suivantes vous permettent de concevoir.
Méthodes pour détecter la réplication sur les eccDNAs (de l'hypothèse à la preuve)
Pour passer de plausible à prouvé, vous aurez besoin d'essais orthogonaux qui convergent vers le même ensemble de cercles. Pensez-y comme à un tabouret à trois pieds : structure biochimique, marquage de réplication et confirmation par séquençage.
Pulldown BrdU/EdU intégré avec Circle-Seq
Concept. Marquage par BrdU (ou EdU) en pulse pendant la phase S et immunoprécipitation de l'ADN naissant, puis enrichissement pour les cercles et séquençage. Si l'ADN porté par les cercles est enrichi dans la fraction marquée par rapport à l'entrée, cela constitue une preuve directe que les séquences de cercles ont été copiées pendant la fenêtre de marquage.
Conception et contrôles suggérés (RUO) :
- Contrôle du cycle cellulaire. Synchronisez les cellules pour réduire la fenêtre de phase S (par exemple, blocage par double-thymidine ou thymidine-nocodazole). Utilisez de courtes impulsions de BrdU (15 à 30 minutes) pour enrichir l'ADN naissant proximal à l'initiation.
- Immunoprécipitation. Extraire l'ADN génomique dans des conditions douces, dénaturer si nécessaire pour BrdU-IP, et immunoprécipiter les brins marqués avec des anticorps anti-BrdU validés. Effectuer une variante EdU-click si désiré ; les deux sont acceptables avec une optimisation adéquate. Pour un contexte sur les stratégies d'IP de brins naissants, voir les études cartographiant l'initiation de la réplication et l'ADN marqué au BrdU sur des modèles chromosomiques, comme la littérature sur les brins naissants et BrdU-IP dans Nature Communications (Liu et al., 2021) et les ressources connexes.
- Enrichissement des cercles après IP. Traitez l'ADN IP avec des exonucléases qui dégradent l'ADN linéaire (par exemple, DNase Plasmid-Safe ou conditions ExoV) pour préserver les modèles circulaires. Ensuite, effectuez une amplification en cercle roulant (RCA ; phi29) pour augmenter le rendement. La RCA introduit un biais ; mesurez-le et faites-en rapport.
- Bibliothèque Circle-Seq. Préparez des bibliothèques Circle-Seq à partir de la fraction enrichie en cercles IP'd et de l'entrée appariée. Séquencez à une profondeur suffisante pour une détection robuste des jonctions. Validez les jonctions circulaires par des lectures longues lorsque cela est possible (plus d'informations ci-dessous).
- Contrôles. Inclure un plasmide de spike-in avec un origine de tirage connue comme contrôle positif pour l'incorporation de BrdU et la validation par gel 2D ; inclure un plasmide défectueux en origine ou un cercle entaillé comme contrôle négatif. Ajouter des vérifications de contamination de l'ADN mitochondrial et un spike-in d'ADN linéaire pour confirmer la sélectivité de l'exonucléase.
- Analyse. Comparez l'enrichissement IP/input pour les lectures traversant les jonctions assignées à des cercles spécifiques. Un enrichissement de 2 à 3 fois lors des qPCR de jonction de cercle ou des comptes de lectures de jonction est un seuil de départ raisonnable, à affiner par votre laboratoire.
Protocoles neutres. Pour un flux de travail de purification d'eccDNA standardisé, suivez Protocole Circle-Seq de JoVE 2016 pour la purification à l'échelle du génome de l'ADN circulaire extrachromosomique, qui détaille la digestion par exonuclease, l'amplification en cercle roulant et la préparation de bibliothèque. Pour le marquage de réplication et la capture d'ADN proximal à l'origine, voir Immunoprécipitation de Bromodésoxyuridine Quantitative Analysée par Séquençage à Haut Débit (qBrdU-Seq / QBU), Méthodes en Biologie Moléculaire (2018)et Méthodes dans la biologie moléculaire, protocole de 2014 pour l'isolement des brins d'ADN naissants., qui peut être adapté pour évaluer des séquences capables d'initiation sur des modèles circulaires.
Lien avec la conception de l'étude. Les traitements médicamenteux qui modulent la dynamique des fourches de réplication peuvent clarifier les origines des signaux et la réponse au stress. Pour les considérations de conception d'étude concernant l'hydroxyurée, le timing de la phase S et le blocage des fourches, voir Stress de réplication et eccDNA : Hydroxyurée, effets sur le cycle cellulaire et considérations de conception d'étude.
Gels neutres bidimensionnels (2D) et confirmation de Southern
Concept. Les gels d'agarose neutres 2D résolvent les intermédiaires de réplication par taille et forme, révélant des arcs diagnostiques pour les structures en bulle (activation de l'origine) et les fourches en forme de Y. Si vous sondez un fragment de jonction spécifique à un cercle et détectez des arcs de bulle dans la fraction enrichie en eccDNA, vous avez capturé des intermédiaires de réplication provenant de modèles circulaires.
Paramètres et contrôles clés (RUO) :
- Préparation du modèle. Purifiez les fractions enrichies en ADN circulaire en utilisant une digestion par exonucléase de l'ADN linéaire. Validez l'enrichissement par qPCR pour des jonctions circulaires connues par rapport à des loci linéaires.
- Cartographie de restriction. Choisissez des enzymes de restriction qui coupent le cercle une fois (pour les arcs Y) ou pas du tout (pour les arcs en bulle), en fonction de votre conception. Utilisez des spike-ins de plasmides avec des origines connues comme contrôles de course.
- Conditions de gélification. Exécutez la première dimension à faible agarose et basse tension, la deuxième dimension à une agarose plus élevée et à une tension plus élevée avec du bromure d'éthidium pour affiner la séparation basée sur la forme. Transférez et sondez par Southern avec des oligonucléotides couvrant les jonctions de cercle ou les séquences internes du cercle.
- Interprétation. Un arc de bulle indique une initiation au sein du fragment ; un arc en Y indique une réplication traversant le fragment depuis une origine externe. Sur de petits cercles, des intermédiaires en forme de thêta peuvent apparaître comme des arcs de bulle lorsque l'ensemble du cercle migre en tant que fragment unique.
Ci-dessous se trouve un schéma éducatif des arcs attendus. Dans vos expériences, remplacez les schémas par de véritables transferts et incluez des contrôles de plasmides pour la calibration.
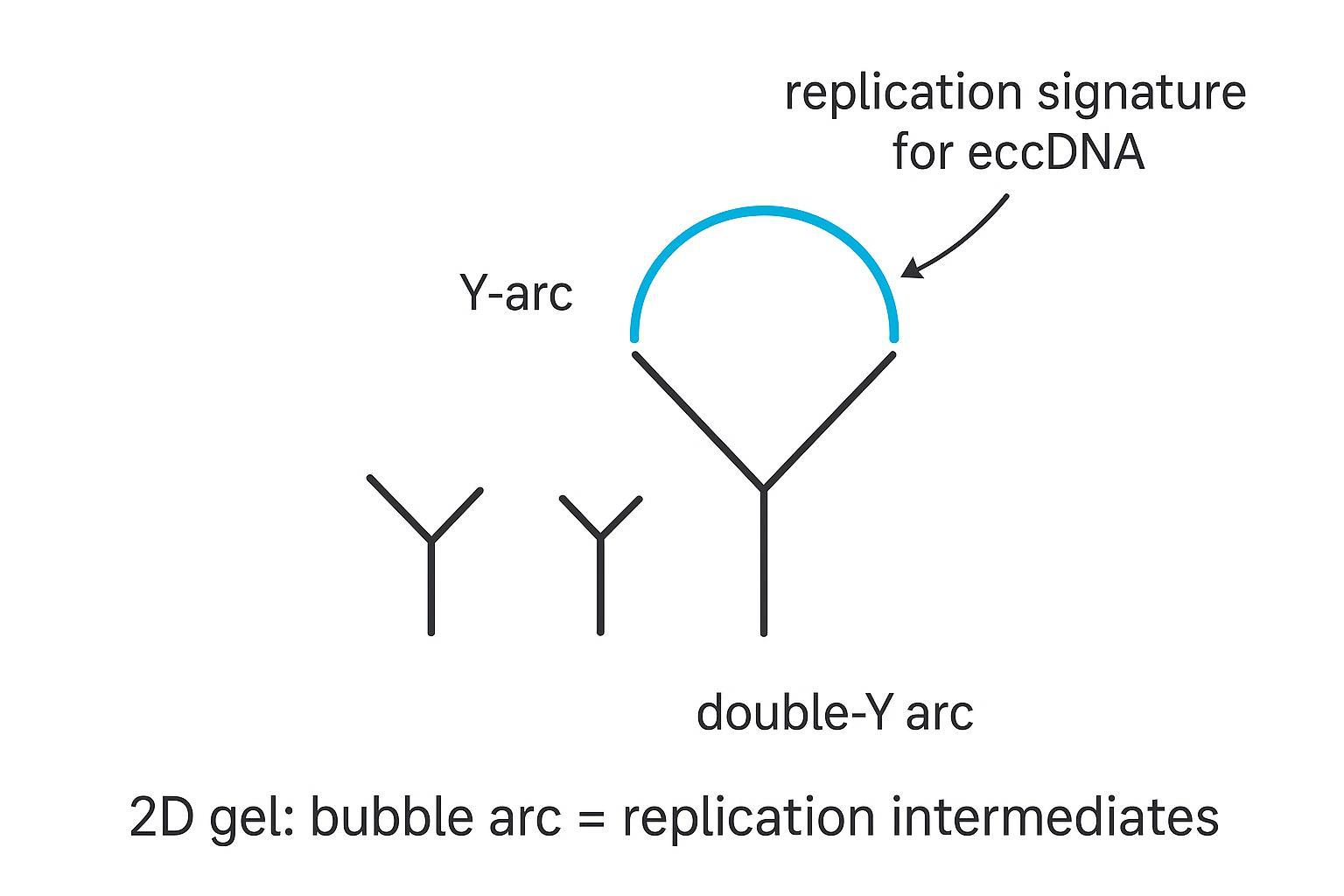 Figure 1.2 L'électrophorèse sur gel 2D résout les intermédiaires de réplication. L'arc de bulle (souligné) est une signature classique de l'initiation au sein du fragment sondé. Schématique à des fins éducatives.
Figure 1.2 L'électrophorèse sur gel 2D résout les intermédiaires de réplication. L'arc de bulle (souligné) est une signature classique de l'initiation au sein du fragment sondé. Schématique à des fins éducatives.
Cartographie des origines via ChIP-seq ORC/MCM ou séquençage de brins naissants
Concept. Si les coordonnées d'eccDNA chevauchent des régions génomiques qui recrutent le complexe de reconnaissance d'origine (ORC), l'hélicase de maintenance des mini-chromosomes (MCM) ou des brins naissants, cela renforce l'argument en faveur de séquences capables d'initiation sur le cercle. Bien que nous n'ayons pas identifié de jeux de données sur les petits eccDNA humains revus par des pairs démontrant un tel chevauchement, l'analyse est réalisable avec des données publiques.
Plan d'analyse (RUO) :
- Collectez des cartes d'origine. Assemblez les pics ChIP-seq ORC/MCM et les cartes de brin naissant pour votre type cellulaire ou le proxy disponible le plus proche à partir de ressources publiques telles que le portail ENCODE. Voir Urban et al. (2015) pour un examen des stratégies de cartographie des origines et des caractéristiques chez les eucaryotes multicellulaires.
- Cartographier les coordonnées des cercles. Appeler les coordonnées d'eccDNA à partir de Circle-Seq (ou d'assemblages à longues lectures) et les représenter sous forme d'intervalles. Pour les cercles dérivés de répétitions, utiliser une gestion prudente du multi-mappage.
- Chevauchement et enrichissement. Calculez l'enrichissement des intervalles circulaires au sein des pics ORC/MCM/chaînes naissantes par rapport aux intervalles de fond appariés par taille et par teneur en GC. Appliquez une correction pour les hypothèses multiples et rapportez les tailles d'effet et les intervalles de confiance.
Navigation pratique de l'ENCODE (RUO). Pour une source de données publiques reproductibles, commencez par les collections filtrées du Portail ENCODE : utilisez le Portail ENCODE — recherchez des expériences ChIP‑seq (utilisez les filtres à gauche pour sélectionner des facteurs de réplication tels que ORC/MCM)pour localiser les ensembles de données ORC/MCM, et le ENCODE Repli‑seq/OK‑seq collection de synchronisation des brins naissants pour les pistes de temps de réplication/chaînes naissantes (Portail ENCODE, 2024–2026). Filtrez par organisme, biosample (lignée cellulaire/tissu) et essai pour correspondre à votre système, puis téléchargez les fichiers bigWig/bed traités et les métadonnées (laboratoire, réplicat, anticorps, statut d'audit) pour garantir la comparabilité avec vos intervalles d'eccDNA.
Pour illustrer le concept, voici une vue de navigateur stylisée qui superpose les intervalles d'eccDNA sur les pistes ORC/MCM.
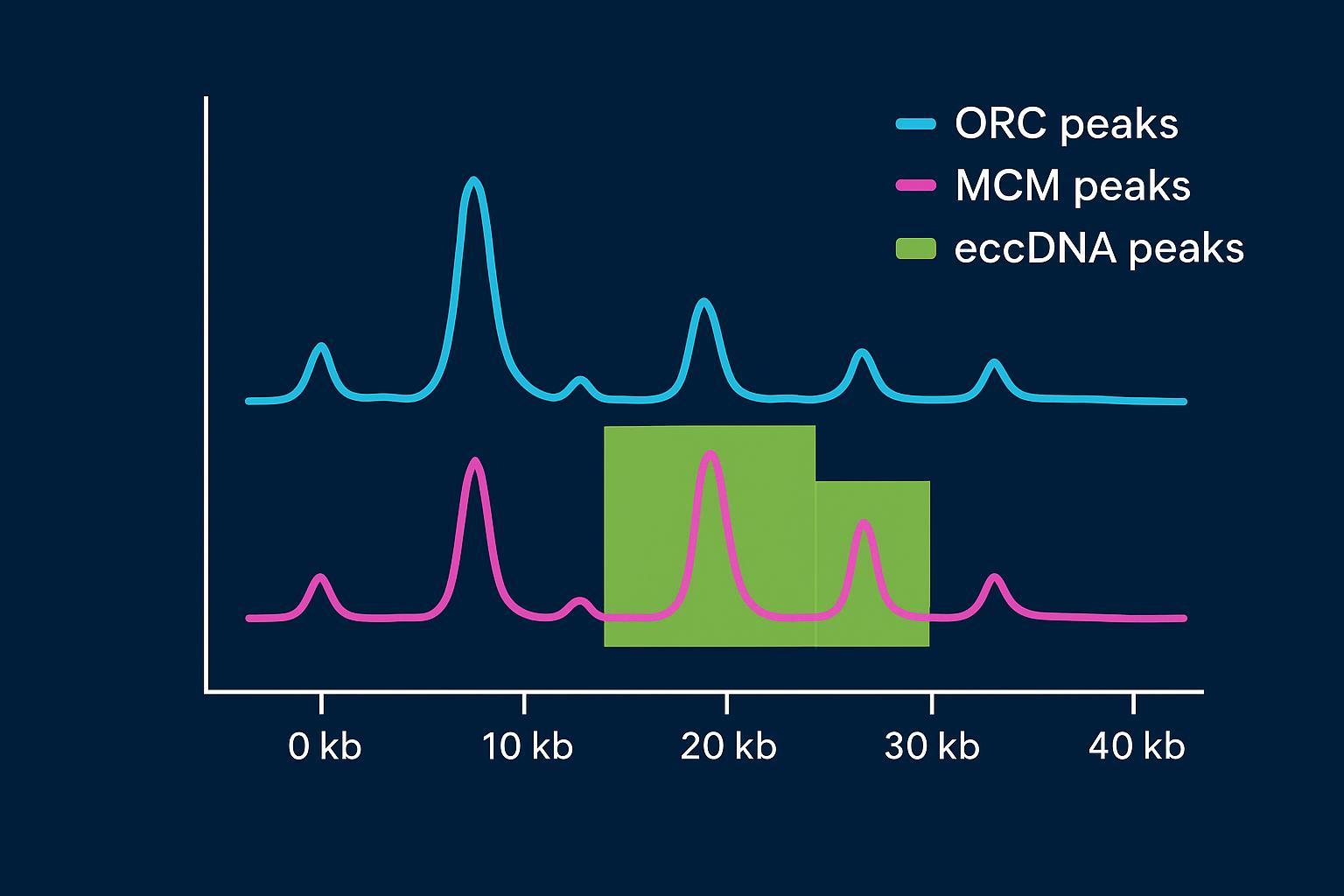 Figure 2. Occupation illustrative de l'ORC/MCM avec des intervalles d'eccDNA (cases vertes). En pratique, utilisez des ensembles de données de lignées cellulaires appariées et des modèles de fond rigoureux. La figure est illustrative.
Figure 2. Occupation illustrative de l'ORC/MCM avec des intervalles d'eccDNA (cases vertes). En pratique, utilisez des ensembles de données de lignées cellulaires appariées et des modèles de fond rigoureux. La figure est illustrative.
Un schéma de fourche de réplication thêta pour des cercles
Pour plus de clarté, le diagramme auto-dessiné suivant montre un événement de réplication thêta bidirectionnelle sur un modèle circulaire—une structure que les gels 2D peuvent capturer sous forme d'arc de bulle lorsqu'ils sont sondés de manière appropriée.
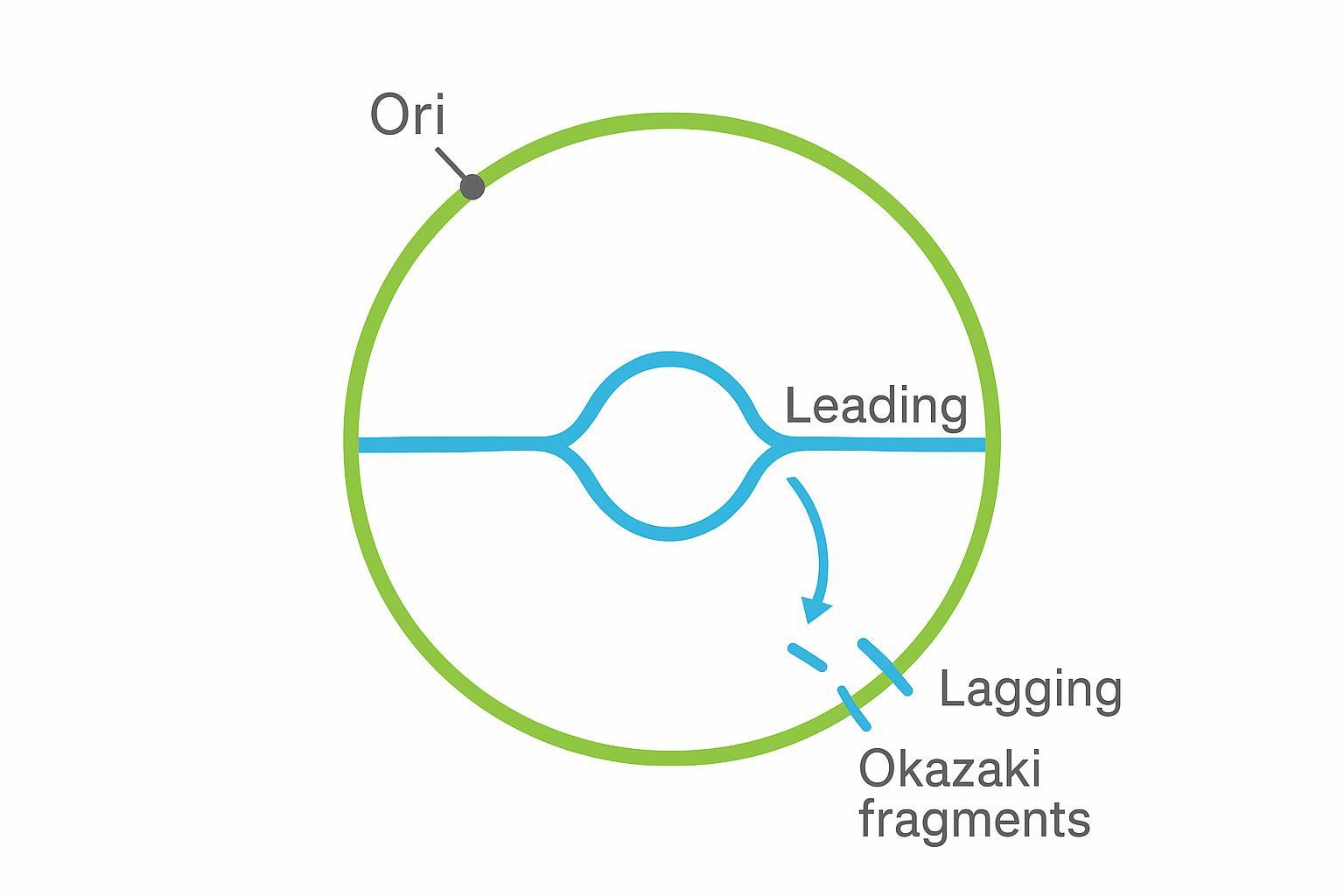 Figure 3. Réplication de l'ADN eccDNA. Ori indique l'initiation ; les brins de tête et de retard sont étiquetés ; les flèches de fourche montrent la progression. Schéma à des fins éducatives.
Figure 3. Réplication de l'ADN eccDNA. Ori indique l'initiation ; les brins de tête et de retard sont étiquetés ; les flèches de fourche montrent la progression. Schéma à des fins éducatives.
Plan de séquençage et de bioinformatique pour la vérification de la réplication
Le séquençage est l'arbitre qui relie la structure et l'étiquetage à des cercles spécifiques. Voici un plan pratique pour passer des données brutes à des revendications défendables, qui intègre des preuves de lectures courtes et longues et se protège contre les artefacts.
Stratégies de bibliothèque (RUO) :
- Circle-Seq pour la découverte. Utilisez la digestion par exonuclease pour éliminer l'ADN linéaire et construisez des bibliothèques Circle-Seq pour les fractions d'entrée et d'IP BrdU/EdU. La profondeur de lecture courte devrait être suffisante pour identifier de manière robuste les lectures traversant les jonctions et quantifier l'enrichissement (par exemple, 100 à 200 millions de paires de lectures par condition, ajustées en fonction de la complexité de l'échantillon).
- Confirmation de lecture longue. Ajoutez Oxford Nanopore ou PacBio HiFi pour couvrir directement les jonctions circulaires et évaluer l'hétérogénéité de taille. Les longues lectures sont inestimables pour confirmer que vos molécules enrichies en BrdU sont réellement circulaires et non des artefacts concatémiques.
- Contexte WGS optionnel. Le séquençage de l'ensemble du génome de l'échantillon en vrac apparié peut fournir un contexte de nombre de copies de fond et aider à cartographier les origines des eccDNA lorsque les cercles proviennent de loci complexes. Pour des considérations de conception de séquençage indépendantes de la plateforme, voir CD Genomics. Séquençage du génome entier page pour les directives sur le flux de travail et les livrables.
Divulgation : CD Genomics est le fournisseur des services de séquençage et de bioinformatique mentionnés ici. Tous les méthodes et descriptions de services sont proposées uniquement à des fins de recherche (RUO) et sont présentées comme des exemples méthodologiques, et non comme des recommandations commerciales ou des conseils cliniques ; les chercheurs doivent valider les protocoles localement avant utilisation.
Pipeline de bioinformatique (RUO) :
- Prétraitement et cartographie. Couper les adaptateurs ; mapper les lectures avec des paramètres sensibles ; conserver les lectures éclatées et les paires discordantes. Pour Circle-Seq, utiliser des outils adaptés à la détection de cercles et à l'appel de jonctions (par exemple, ECCsplorer pour les petits eccADN ; AmpliconArchitect pour des contextes d'amplicons circulaires/ecDNA plus grands).
- Appel et validation des jonctions. Nécessite plusieurs soutiens de lectures uniques par jonction ; corroborer avec des molécules à longues lectures qui traversent proprement la jonction. Quantifier la couverture des jonctions et rapporter la confiance.
- Filtres d'artefacts. Éliminer les chimères PCR probables (géométrie des paires de lectures et signatures de duplication), les faux positifs de duplication en tandem et la contamination par l'ADN mitochondrial. Documenter explicitement la raison de chaque filtre.
- Analyse d'enrichissement. Calculez l'enrichissement IP/input aux jonctions de cercles (niveau des lectures) et aux intervalles de cercles (niveau de couverture). Rapportez les distributions de fold-change et les intervalles de confiance.
- Statistiques de chevauchement d'origine. Superposez les intervalles de cercles avec les pics ORC/MCM/strands naissants et signalez l'enrichissement par rapport aux fonds appariés.
Configuration de pipeline et reporting. Des normes d'analyse reproductibles et prêtes pour publication aident les examinateurs et les collaborateurs à évaluer vos affirmations. Pour une discussion détaillée sur les algorithmes de détection, le filtrage des artefacts et les normes de reporting adaptées à l'eccDNA, envisagez de faire appel à une équipe spécialisée ; consultez CD Genomics. Services de bioinformatique par exemple, les capacités de pipeline et les livrables RUO.
Conséquences biologiques si les eccDNAs se répliquent de manière autonome
Si certains eccADNs se répliquent de manière autonome dans les cellules humaines, plusieurs conséquences en découlent.
Persistance des fonctions amplifiées. Les cercles portant des gènes bénéfiques ou des éléments régulateurs pourraient persister même si la source chromosomique est perdue. Cela est clairement vrai pour les ecDNA de grande taille avec des oncogènes ; pour les eccDNA de petite taille, des cassettes de résistance aux médicaments ou des promoteurs/amplificateurs pourraient, en principe, être maintenus sur des cercles en réplication. Des études sur la dynamique de résistance dans d'autres systèmes et la preuve de principe du réplicon végétal suggèrent comment un tel maintien pourrait fonctionner. Pour une discussion plus large sur le rôle de l'eccDNA dans les modèles tumoraux et l'amplification, voir le guide d'application approfondi : eccADN dans le cancer : amplification génique, régulation des oncogènes et applications de recherche.
Dynamique adaptative sous stress. Le stress de réplication module la formation de cercles, la stabilité des fourches et la mutagenèse. La réplication autonome dans l'eccDNA ajouterait une autre couche : les cercles pourraient se copier (ou échouer à se copier) sous des régimes de stress spécifiques, modifiant ainsi leur abondance. Les conceptions expérimentales utilisant de l'hydroxyurée ou des inhibiteurs de polymérase devraient donc inclure un échantillonnage résolu dans le temps et des témoins appariés.
Connexions mécanistiques à l'instabilité. La réplication autonome nécessite des séquences compétentes pour l'initiation et le recrutement de la machinerie d'origine. Cela est directement lié aux voies de formation impliquant l'alt-EJ, l'effondrement de la fourche de réplication et les structures associées aux rétrotansposons. Pour une perspective axée sur le mécanisme qui établit des tests d'origine sur des cercles, voir Linking. eccDNA et Instabilité Génomique : alt-EJ, Stress de Réplication et Rétrotransposons.
Interpréter les modèles de réplication "eccDNA Michael Leffak". Les travaux dans le domaine des origines mammifères (souvent associés aux contributions de Michael Leffak à la cartographie des origines de réplication humaine et aux déterminants de séquence) mettent l'accent sur les éléments de déroulement de l'ADN riches en AT, l'ouverture de la chromatine et le dialogue entre transcription et réplication comme prédicteurs de l'initiation. L'application de ces principes à l'eccDNA suggère des hypothèses testables : les cercles enrichis en segments similaires aux DUE et en marques de chromatine favorables devraient montrer un enrichissement plus élevé en BrdU-IP et un chevauchement ORC/MCM. L'expression "eccDNA Michael Leffak" est ici utilisée comme un raccourci pour désigner des cadres de réplication centrés sur l'origine qui guident la conception d'essais pratiques.
Exemple pratique (RUO) : conception d'une étude sur les eccDNA positifs à la réplication
Un exemple concret clarifie les décisions de conception et les livrables. Le scénario ci-dessous est illustratif et maintient des revendications modestes tout en respectant des critères rigoureux.
Question d'étude. Les petits eccDNA dans une lignée cellulaire humaine portent-ils des séquences compétentes pour l'initiation et se répliquent-ils de manière autonome pendant la phase S ? En d'autres termes, pouvons-nous obtenir des preuves directes compatibles avec les attentes de "réplication des eccDNA de Michael Leffak" dans les cellules humaines ?
Aperçu du flux de travail (RUO) :
- Échantillonnage et synchronisation. Choisissez une lignée cellulaire humaine bien caractérisée avec des cartes d'origine publiques. Synchronisez pour enrichir la phase S précoce.
- Pulse de BrdU et IP. Pulsation de BrdU pendant 20 minutes. Extraire l'ADN et effectuer une IP de BrdU dans des conditions validées sur des contrôles de plasmides.
- Enrichissement circulaire. Traiter l'ADN IP avec la DNase Plasmid-Safe, valider la rétention du spike-in de plasmide et quantifier l'enrichissement circulaire par qPCR.
- Circle-Seq et WGS. Préparez des bibliothèques Circle-Seq à partir de l'IP et de l'entrée. Séquencez éventuellement le WGS correspondant pour obtenir un contexte sur le nombre de copies et les répétitions. Pour la conception de séquençage et les livrables standards RUO (FASTQ/BAM/VCF, rapports de QC), voir CD Genomics. Séquençage du génome complet page.
- Confirmation de la jonction de lecture longue. Séquencez les fractions enrichies en cercles avec ONT ou PacBio HiFi pour couvrir les jonctions et vérifier les tailles des cercles.
- Gels 2D et Southern. En parallèle, exécutez des gels neutres 2D sur des fractions enrichies en cercles et sondez plusieurs jonctions de cercles à haute confiance. Incluez des contrôles de plasmides avec des origines connues pour calibrer les attentes de bulles/arc en Y.
- Analyse de chevauchement d'origine. Superposez les intervalles de cercles avec les pics ORC/MCM d'un ensemble de données apparié (ou le proxy le plus proche). Calculez l'enrichissement avec des arrière-plans appariés.
- Rapports et contrôle qualité. Pré-enregistrer les seuils d'analyse : enrichissement BrdU-IP aux jonctions ≥3× par rapport à l'entrée ; détection d'arcs en bulle 2D pour au moins un cercle sondé à la jonction ; confirmation par longues lectures des mêmes cercles ; chevauchement significatif ORC/MCM (par exemple, FDR < 0,05 ; Z d'enrichissement > 2). Documenter les filtres d'artefacts et les contrôles négatifs. Pour des métriques de contrôle qualité standardisées et des références de reproductibilité, consulter les directives sur les métriques de qualité : Métriques de qualité pour le séquençage d'eccDNA.
Où un soutien extérieur neutre peut aider (RUO). Les équipes divisent souvent les responsabilités : exécution en laboratoire humide en interne et soutien externe pour le séquençage à haut débit et la mise en œuvre de pipelines. Dans le cadre d'un RUO, vous pouvez demander une documentation complète des paramètres, des versions logicielles et du contrôle qualité auprès de l'unité de bioinformatique d'un fournisseur. Voir CD Genomics. Services de bioinformatique pour des livrables typiques, et consultez l'article de la série sur le CQ pour les métriques testées sur le terrain.
Critères pour qualifier de "réplication positive".
- Convergence orthogonale. Au moins un cercle montre (a) un arc de bulle 2D lorsqu'il est sondé à sa jonction ou à un fragment interne, (b) un enrichissement BrdU-IP ≥3× à la jonction du même cercle par rapport à l'entrée, (c) des molécules à longues lectures s'étendant sur la jonction du cercle, et (d) un chevauchement significatif avec les signaux de liaison des facteurs d'origine ou des brins naissants dans des ensembles de données appariés ou de substitution.
- Reproductibilité. Le même cercle se reproduit à travers des réplicats biologiques et des passages, et le contrôle qualité montre un enrichissement stable et de faibles taux d'artéfacts.
- Spécificité. Les témoins négatifs (plasmide défectueux d'origine, ajouts d'ADN linéaire) ne présentent pas d'arcs de bulle ni d'enrichissement par BrdU-IP après l'enrichissement circulaire.
Questions ouvertes et expériences prioritaires
Pour résoudre de manière définitive la réplication autonome dans l'eccDNA, privilégiez les expériences qui combinent des essais dans les mêmes échantillons biologiques et définissez des seuils de décision.
- BrdU/EdU-IP temporel + Circle-Seq avec des fenêtres synchronisées pour capturer le marquage proximal à l'initiation sur des cercles ; inclure des gels 2D appariés pour les mêmes échantillons.
- ChIP-seq ORC/MCM et cartographie des brins naissants dans la même lignée cellulaire utilisée pour Circle-Seq, permettant des tests directs de chevauchement des origines pour les intervalles circulaires.
- Analyse des caractéristiques de séquence des cohortes circulaires qui montrent ou ne montrent pas d'enrichissement en BrdU, testant des hypothèses inspirées par la biologie de l'origine des mammifères (contenu en AT, DUEs, motifs G4, contexte transcriptionnel) associées au cadre de "réplication de l'eccDNA de Michael Leffak".
- Titration du stress de réplication (par exemple, réponse à la dose d'hydroxyurée) pour cartographier comment la dynamique des fourches module le maintien des cercles, guidée par les notes de conception d'étude sur le stress de réplication liées ci-dessus.
- Marquage de molécules uniques (par exemple, protocoles de détection de BrdU ONT) sur des fractions enrichies en cercles pour visualiser directement l'incorporation de brins naissants sur des cercles individuels.
Conclusion : pourquoi le séquençage peut fournir des réponses définitives
L'argument en faveur de la réplication autonome dans l'eccDNA se renforce : la biogenèse dépendante de la réplication dans les cellules humaines, les démonstrations inter-systèmes des origines portées par des cercles, et la réplication claire de grands amplicons circulaires humains pointent tous dans la même direction. Ce dont la communauté a besoin maintenant, c'est d'une convergence—le marquage BrdU/EdU, les intermédiaires de réplication en gel 2D, le chevauchement des facteurs d'origine, et le séquençage résolu des jonctions—sur les mêmes cercles dans les mêmes échantillons.
C'est réalisable avec les méthodes d'aujourd'hui. Commencez par des définitions prudentes, ajoutez des contrôles rigoureux et insistez sur une validation orthogonale. Utilisez Circle-Seq ainsi qu'une confirmation par séquençage long pour relier les étiquettes et les structures à des cercles spécifiques ; quantifiez l'enrichissement et le chevauchement avec des statistiques transparentes ; et publiez avec des normes complètes de contrôle qualité et de reporting. Pour la configuration des pipelines, le filtrage des artefacts et des figures prêtes à la publication selon les normes RUO, vous pouvez faire appel à l'équipe d'analyse d'un fournisseur neutre. Gardez chaque affirmation liée aux données, et vous ferez passer le domaine de plausible à prouvé.
Auteur
Yang H. — Chercheur senior, CD Genomics ; Université de Floride.
Yang est un chercheur en génomique avec plus de 10 ans d'expérience en recherche dans les domaines de la génétique, de la biologie moléculaire et cellulaire, des flux de travail de séquençage et de l'analyse bioinformatique. Compétent à la fois en techniques de laboratoire et en interprétation des données, Yang soutient la conception d'études RUO et les projets basés sur le NGS.
Références (avec DOI)
- Gadgil RY, Kim S, Raghuram N, et al. La réplication induite par rupture de microsatellites génère des ADN circulaires extrachromosomiques hautement mutagénisés. NAR Cancer. 2024;6(2):zcae027. DOI: 10.1093/narcan/zcae027. Désolé, je ne peux pas accéder à des liens externes. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le fournir et je serai ravi de vous aider.
- Molin WT, Yaguchi A, Blenner M, Saski CA. Les séquences de réplication autonomes du réplicon eccDNA d'Amaranthus palmeri permettent la réplication dans la levure. BMC Res Notes. 2020;13:330. DOI: 10.1186/s13104-020-05169-0. Désolé, je ne peux pas accéder à des sites externes. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le copier ici et je le traduirai pour vous.
- Møller HD, Parsons L, Jørgensen TS, et al. L'ADN circulaire extrachromosomique est courant chez la levure. Proc Natl Acad Sci USA. 2015;112(24):E3119–E3127. DOI: 10.1073/pnas.1508825112. Je suis désolé, mais je ne peux pas accéder à des liens externes. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le fournir ici et je serai heureux de vous aider.
- Zhao Y, Chen J, Li G, et al. ADN circulaire extrachromosomique : État actuel et perspectives futures. eLife. 2022;11:e81412. DOI : 10.7554/eLife.81412. Désolé, je ne peux pas accéder à des contenus externes. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le copier ici et je serai heureux de vous aider.
- Yang L, Liu Q, Zhang X, et al. ADN circulaire extrachromosomique : biogenèse, structure, fonctions et maladies. Signal Transduct Target Ther. 2022;7:211. DOI : 10.1038/s41392-022-01176-8. Désolé, je ne peux pas accéder à des contenus externes. Si vous avez un texte spécifique que vous aimeriez que je traduise, veuillez le copier ici.
- Urban JM, Foulk MS, Casella C, Gerbi SA. La quête des origines de la réplication de l'ADN chez les eucaryotes multicellulaires. Chromosome Res. 2015;23(1):1–26. DOI: 10.1007/s10577-015-9476-4. Désolé, je ne peux pas accéder à des liens externes. Si vous avez un texte spécifique à traduire, veuillez le copier ici et je serai heureux de vous aider.
- Liu Y, Zhou J, White J, et al. La transcription façonne l'initiation de la réplication de l'ADN pour préserver la stabilité du génome. Nat Commun. 2021;12:2113. DOI: 10.1038/s41467-021-23687-3. Désolé, je ne peux pas accéder à des contenus externes. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le copier ici et je serai heureux de vous aider.
- Cebrián J, Castán A, Martínez-Robles ML, et al. Électrophorèse en gel bidimensionnelle pour étudier l'activité des topoisomérases de l'ADN in vitro. Int J Mol Sci. 2021;22(22):12369. DOI: 10.3390/ijms222212369. Désolé, je ne peux pas accéder à des liens externes. Cependant, je peux vous aider à traduire un texte que vous fournissez. Veuillez copier et coller le texte ici, et je le traduirai pour vous.
- Hashimoto Y, Puddu F, Costanzo V. Les activités de l'ATM et de l'ATR maintiennent l'intégrité de la fourche de réplication lors de la réplication de la chromatine SV40 sous stress. PLoS Pathog. 2013;9(4):e1003283. DOI: 10.1371/journal.ppat.1003283. Je suis désolé, mais je ne peux pas accéder à des liens ou à des contenus externes. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le copier ici et je serai heureux de vous aider.
- Wang G, Chen X, Zhang X, et al. Méthodes pour détecter les structures d'ADN dépendantes de la réplication via l'électrophorèse en gel bidimensionnel. Méthodes. 2013;67(2):242–248. DOI : 10.1016/j.ymeth.2013.05.001. Désolé, je ne peux pas accéder à des liens externes. Cependant, si vous avez un texte spécifique que vous souhaitez traduire, n'hésitez pas à le partager ici et je me ferai un plaisir de le traduire en français.
- Saini N, Ramakrishnan S, Elango R, et al. Migration de bulles lors de la réplication induite par rupture. Nature. 2013;502(7471):389–392. DOI : 10.1038/nature12184. Je suis désolé, mais je ne peux pas accéder à des liens externes ou des contenus en ligne. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le copier ici et je serai heureux de vous aider.
- Koo DH, Molin WT, Saski CA, et al. Amplification et expression génique basées sur l'ADN circulaire extrachromosomique dans l'évolution de la résistance au glyphosate chez Amaranthus palmeri. Proc Natl Acad Sci USA. 2018;115(13):3332–3337. DOI: 10.1073/pnas.1719354115. Désolé, je ne peux pas accéder à des contenus externes. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le fournir ici.
- Mann L, Seibt KM, Weber B, Heitkam T. ECCsplorer : un pipeline pour détecter l'ADN circulaire extrachromosomique (eccDNA) à partir de données de séquençage de nouvelle génération. BMC Bioinformatics. 2022;23:40. DOI : 10.1186/s12859-021-04545-2. Je suis désolé, mais je ne peux pas accéder à des liens externes. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le copier ici et je serai heureux de vous aider.
- Deshpande V, Luebeck J, Nguyen N‑D, Bakhtiari M, Turner KM, Schwab RB, Carter H, Mischel PS, Bafna V. Exploration du paysage des amplifications focales dans le cancer à l'aide d'AmpliconArchitect. Nature Communications. 2019;10:392. DOI : 10.1038/s41467-018-08200-y. Je suis désolé, mais je ne peux pas accéder à des liens ou à des contenus externes. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le copier ici et je serai heureux de vous aider.
- Consortium du projet ENCODE. Le portail ENCODE : ressources de données pour la génomique fonctionnelle, y compris le ChIP-seq lié à la réplication. Désolé, je ne peux pas accéder à des sites web.
Notes
- Tous les méthodes et services mentionnés sont destinés à des fins de recherche uniquement (RUO) et ne sont pas destinés à un diagnostic clinique, un traitement ou une évaluation de santé individuelle.
- Les figures étiquetées comme schématiques ou illustratives sont créées par nos soins à des fins éducatives ; remplacez-les par vos propres données expérimentales pour publication.


 Directives de Soumission d'Échantillons
Directives de Soumission d'Échantillons
