Des signaux bruts aux Fastq : Naviguer dans les exigences GPU et l'infrastructure pour le basecalling Nanopore
Les études sur le microbiome deviennent rarement difficiles à défendre en raison d'un manque de résultats de séquençage. Elles deviennent difficiles à défendre parce que les résultats ne peuvent pas être entièrement retracés à un flux de travail contrôlé. Dans les recherches en phase de révision, les examinateurs remettent souvent en question si la structure de la communauté rapportée reflète les échantillons eux-mêmes ou le comportement technique cumulatif de la collecte, de l'extraction, du choix des amorces, de l'amplification, du séquençage et de l'analyse. De grandes études de comparaison de flux de travail et des articles méthodologiques continuent de montrer que les profils microbiens sont sensibles aux variations techniques tout au long de la chaîne, de la collecte des échantillons au séquençage et au traitement en aval.
L'anatomie du biais des amorces : choisir la bonne cible pour votre environnement
V3-V4 reste le choix par défaut le plus familier dans de nombreuses études sur le microbiome, mais la familiarité n'est pas synonyme de neutralité. Une région variable est un choix de conception qui influence ce qui est amplifié efficacement, ce qui est classé avec confiance et ce qui est systématiquement sous-représenté. Des travaux comparatifs récents montrent que le pouvoir discriminatoire varie considérablement selon les régions variables et les genres, ce qui signifie qu'une région couramment utilisée peut bien fonctionner dans un environnement tout en sous-performant dans un autre.
 Figure 1. Le choix de la région variable modifie à la fois la largeur de couverture et la résolution taxonomique. Le même environnement d'étude peut donner des profils de récupération différents selon que l'on utilise V3-V4, plusieurs régions ou le 16S complet.
Figure 1. Le choix de la région variable modifie à la fois la largeur de couverture et la résolution taxonomique. Le même environnement d'étude peut donner des profils de récupération différents selon que l'on utilise V3-V4, plusieurs régions ou le 16S complet.
Le biais de primer se manifeste généralement de cinq manières. Premièrement, un taxon biologiquement important est systématiquement inférieur aux attentes par rapport aux études antérieures ou aux mesures orthogonales. Deuxièmement, des organismes étroitement liés se regroupent sous des étiquettes plus larges parce que la région manque d'informations discriminatoires suffisantes. Troisièmement, des échantillons provenant d'environnements distincts semblent plus similaires qu'ils ne devraient l'être parce que certaines lignées ont été faiblement capturées dès le départ. Quatrièmement, les répliques semblent stables, mais la stabilité reflète un biais d'amplification partagé plutôt qu'une récupération fidèle. Cinquièmement, les statistiques en aval semblent bien se comporter même si la principale distorsion est intervenue avant la normalisation.
Pourquoi V3-V4 est toujours utile, mais pas universellement sûr.
V3-V4 est souvent acceptable lorsque la question d'étude est large, que les taxons attendus sont déjà connus pour être récupérables avec cette région, que le manuscrit ne repose pas sur une séparation taxonomique fine, et que le projet privilégie le débit, le temps de réponse et la simplicité analytique. Cela devient plus risqué lorsque l'environnement d'échantillonnage est taxonomiquement complexe, lorsque la conclusion clé dépend de quelques taxons sensibles, lorsque la communauté cible est mal représentée dans les habitudes de référence courantes, ou lorsque les examinateurs remettent déjà en question la reproductibilité.
C'est à ce moment-là que la refonte de l'objectif devient plus précieuse que de simplement générer plus de lectures. Dans ces cas, un flux de travail de séquençage d'amplicons 16S/18S/ITS en longueur complète peut réduire l'ambiguïté, et un stratégie de séquençage shotgun métagénomique peut éviter complètement la récupération taxonomique limitée à une région lorsque l'étude nécessite un contexte génomique plus large.
Multi-région contre 16S plein longueur : le véritable compromis
Cette décision est souvent décrite comme un choix entre coût et résolution, mais cette formulation est trop étroite. Le compromis réel implique la portée de la couverture, la profondeur discriminatoire, la tolérance à la qualité des entrées, l'adéquation de la base de données de référence, la charge d'analyse et la valeur de révision. Des travaux récents en 16S de longueur complète soutiennent l'idée que des cibles plus longues peuvent améliorer la résolution taxonomique, mais cela n'élimine pas le besoin d'une bonne conception de primers, d'un choix de références robuste et d'un contrôle discipliné du flux de travail.
Une règle de décision pratique est :
- Utilisez V3-V4 lorsque la revendication est large et que les taxons d'intérêt sont connus pour être capturés de manière fiable.
- Utilisez le séquençage multi-régional ou le séquençage complet de l'ARNr 16S lorsque la principale préoccupation est la sous-représentation, l'annotation ambiguë ou l'absence spécifique à l'environnement.
- Escalade au-delà de la logique d'amplicon standard lorsque l'interprétation sensible à la charge ou le contexte génomique sont plus importants que la classification au niveau régional seule.
Pour les projets qui nécessitent une quantification plus précise ou un contexte génomique plus riche, séquençage d'amplicons 16S/18S/ITS quantitatif absolu ou séquençage métagénomique à lecture longue peut être plus informatif que de traiter un essai d'amplicon court comme la réponse universelle.
Effets de lot : Identifier et minimiser le bruit systématique
Si le biais de l'amorce change ce qui entre dans l'ensemble de données, les effets de lot changent la manière dont cela entre de manière reproductible au fil du temps, des sites, des opérateurs, des lots de réactifs et des séquences. Dans les études de microbiome, cela est particulièrement important car les tableaux de comptage sont rares, compositionnels et souvent gonflés de zéros. C'est une des raisons pour lesquelles des méthodes spécifiques aux microbiomes, telles que ConQuR, ont été proposées : les approches de correction de style omique courantes ne modélisent pas toujours suffisamment bien le comportement des comptages de microbiomes par elles-mêmes.
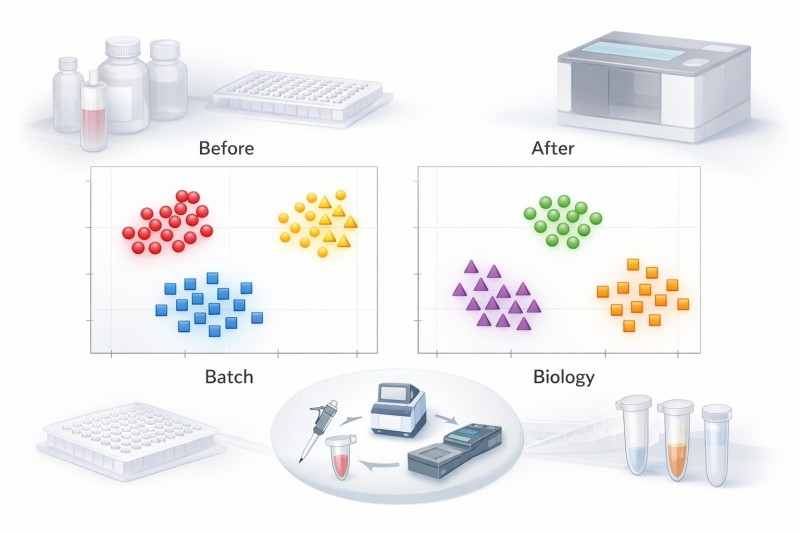 Figure 2. La structure de lot peut dominer l'ordination même après une normalisation simple. Comparez le regroupement en traitant le lot avant une gestion consciente du contrôle et le regroupement par biologie après un prétraitement standardisé et une révision.
Figure 2. La structure de lot peut dominer l'ordination même après une normalisation simple. Comparez le regroupement en traitant le lot avant une gestion consciente du contrôle et le regroupement par biologie après un prétraitement standardisé et une révision.
Les sources les plus courantes de structure par lots
Le bruit de lot dans le travail sur le microbiome provient généralement d'une combinaison de facteurs plutôt que d'un échec évident. Les contributeurs courants incluent la contamination de fond des kits d'extraction, les différences d'intensité de lyse, la variation du nombre de cycles de PCR, les incohérences d'indexation, les variations de séquençage d'un lot à l'autre, les fenêtres de traitement décalées et des métadonnées incomplètes qui empêchent les modèles ultérieurs de distinguer la structure technique de la structure biologique.
Les signes d'avertissement sont généralement reconnaissables avant qu'un modèle de correction formel ne soit appliqué. Les échantillons peuvent d'abord se regrouper par date de traitement ou par ID de course. Les contrôles négatifs peuvent contenir des taxons répétés qui ne ressemblent pas à du bruit aléatoire. Un lot peut provoquer la séparation la plus forte dans l'espace de la bêta-diversité. Les répliques peuvent sembler cohérentes au sein d'une course mais instables entre les courses. Les variations de la diversité alpha peuvent disparaître après une inspection stratifiée par lot. Aucun de ces signaux ne prouve que l'étude est invalide, mais tous indiquent que la biologie rapportée peut ne pas encore être la force organisatrice dominante.
Pourquoi la normalisation ne suffit-elle pas ?
La normalisation redimensionne les comptages. Elle ne supprime pas, à elle seule, la distorsion technique structurée. Si un lot modifie la récupération des taxons en amont, la normalisation peut rendre le tableau plus propre tout en préservant le biais qui est le plus important pour l'interprétation. C'est pourquoi les examinateurs demandent des contrôles et l'historique des processus, pas seulement des graphiques d'abondance re-tracés.
Une règle opérationnelle utile est d'essayer de gérer des lots formels uniquement lorsque trois conditions sont remplies. La variable de lot doit être enregistrée clairement. Des contrôles doivent exister afin que le schéma technique soit observable. Et le groupe biologique d'intérêt ne doit pas être complètement confondu avec le lot. Si tous les échantillons de comparaison ont été traités en une seule fois et tous les contrôles dans une autre, la correction en aval ne peut pas entièrement récupérer l'interprétabilité ; la réponse la plus forte est la redéfinition, des revendications limitées ou un complément clairement qualifié.
Lorsque des inserts plus longs ou des taxons difficiles sont impliqués, des stratégies d'amplicons à longues lectures peuvent améliorer la conception des cibles, mais elles ne suppriment pas la nécessité d'une discipline de lot. A approche de séquençage d'amplicons par nanopore peut aider du côté de la lecture-conception, mais pas du côté de la conception de contrôle.
Normes d'or de contrôle de la qualité : Communautés simulées et Spike-ins
Un flux de travail de microbiome défendable ne se contente pas de rapporter des résultats. Il démontre la qualité de récupération. C'est là que les communautés factices et les ajouts deviennent indispensables plutôt que simplement souhaitables.
Les communautés fictives sont particulièrement précieuses car elles fournissent une composition connue qui passe par la même chaîne d'extraction, d'amplification, de séquençage et d'analyse que les échantillons de recherche. Des études récentes montrent que les contrôles fictifs peuvent révéler des distorsions, identifier des valeurs aberrantes, établir des références pour la variabilité inter-laboratoires et bioinformatique, et exposer des biais spécifiques aux flux de travail que les conceptions basées uniquement sur des échantillons manquent souvent.
Ce qu'une fausse communauté devrait prouver.
Un mock est le plus utile lorsqu'il répond à des questions concrètes de contrôle qualité :
- La composition attendue a-t-elle été récupérée dans une bande de tolérance prédéfinie ?
- Les membres à faible abondance ont-ils été perdus de manière disproportionnée ?
- La contamination est-elle entrée avant l'extraction, pendant l'amplification ou lors de la manipulation de la bibliothèque ?
- Le pipeline de bioinformatique a-t-il créé des faux positifs ou effacé des membres attendus ?
- Les différents lots ont-ils récupéré le mock de manière comparable ?
Pour le travail de révision, ce dernier point est très important. Un évaluateur qui doute de la différence biologique rapportée se demande souvent si la chaîne technique a suffisamment bien fonctionné pour faire confiance à la comparaison.
Les spike-ins traitent d'un problème différent. L'abondance relative peut être interne cohérente mais rester trompeuse quant à la charge microbienne totale. Les standards externes aident à ancrer l'interprétation lorsque la biomasse diffère matériellement entre les échantillons ou lorsque le manuscrit a besoin d'un soutien plus fort pour prouver qu'un changement de composition n'est pas seulement un effet de dénominateur. Dans ces situations, un service de séquençage métagénomique absolu peut être un ajustement plus direct que de se fier uniquement à la logique de l'abondance relative.
Mock contre spike-in : quel contrôle résout quel problème
Utilisez une communauté fictive lorsque la question principale est la fidélité du flux de travail.
Utilisez un spike-in lorsque la question principale est l'ancrage d'abondance.
Utilisez les deux lorsque l'étude doit défendre à la fois la qualité de la récupération et la comparabilité entre les échantillons.
La conception du contrôle devient également plus crédible lorsqu'elle est associée à un chemin de reporting standardisé plutôt qu'improvisé à la fin du projet. Les équipes qui travaillent régulièrement avec des conceptions multicentriques ou à long terme bénéficient souvent de définitions préétablies. Séquençage d'amplicons 16S/18S/ITS flux de travail et fixe séquençage métatranscriptomique conventions de rapport lorsque le contexte transcriptionnel est nécessaire en parallèle du profilage communautaire.
Intégration des données : Des lectures brutes aux résultats à l'épreuve des révisions
Les métadonnées ne sont pas une charge administrative. C'est la structure qui détermine si l'interprétation par lots est possible ultérieurement. Si le kit d'extraction, l'opérateur, la date, le lot de primers, le nombre de cycles PCR, l'ID de course, le placement du contrôle et la version du pipeline sont enregistrés de manière incohérente, alors la "correction par lots" devient une conjecture plutôt qu'une analyse.
Un flux de travail de reporting en bioinformatique prêt pour révision devrait rendre les versions de pipeline, la logique de filtrage, les choix de base de données et les décisions de contrôle qualité figés, traçables et faciles à rapporter.
Métadonnées minimales qui devraient accompagner un ensemble de données sur le microbiome défendable.
Au minimum, le dossier du projet devrait inclure :
- type d'échantillon et conditions de stockage,
- extraction chimie ou version kit,
- conditions de lyse,
- ensemble de amorces et région cible,
- Numéro de cycle PCR et stratégie d'indexation,
- date et lot de préparation de bibliothèque,
- plateforme de séquençage et ID d'exécution,
- emplacements des contrôles négatifs, des contrôles positifs et des matériaux témoins,
- critères de décontamination et de filtration,
- version de pipeline d'analyse.
C'est également à ce stade que de nombreuses équipes découvrent que la modélisation par lots n'est aussi crédible que la discipline de gestion des données en amont. Lorsqu'une étude nécessite un contexte plus large que ce qu'un seul essai peut fournir, soutien aux services multi-omiques peut être plus défendable que de retraiter sans cesse le même type de données étroit en quête de certitude.
Ce qu'un rapport de contrôle qualité transparent devrait montrer
Un rapport QC transparent devrait inclure les comptes de lecture avant et après filtrage, le comportement des échantillons témoins, la récupération simulée par rapport à la composition attendue, l'examen de la contamination à partir des blancs ou des contrôles sans modèle, les diagnostics d'ordination avant et après l'examen tenant compte des lots, les critères pour éliminer les échantillons à faible profondeur ou contaminés, et un tableau final d'inclusion des échantillons.
Tout aussi important, le rapport devrait définir la limite extérieure de l'interprétation. Il devrait indiquer ce que la correction peut aborder et ce qu'elle ne peut pas. Les évaluateurs ont tendance à faire davantage confiance à une affirmation limitée qu'à une affirmation trop étendue.
Évaluation de la qualité des projets sur le microbiome
L'acceptation du projet ne devrait pas être définie par le fait que le séquençage ait été terminé à temps. Elle devrait être définie par le fait que l'ambiguïté technique a été suffisamment réduite pour que la revendication biologique soit interprétable.
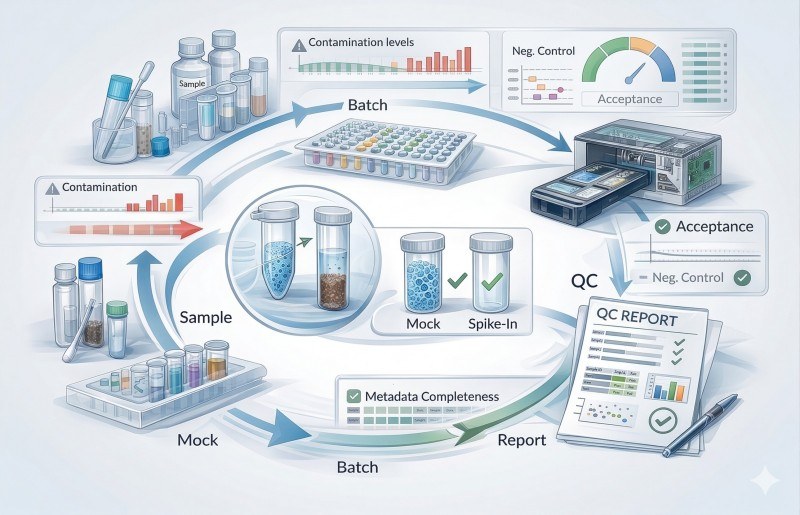 Figure 3. Un flux de travail QC en boucle fermée relie l'entrée des échantillons, les contrôles, le séquençage, l'examen de la contamination, l'évaluation des lots et le rapport final afin que l'ambiguïté technique soit documentée avant l'interprétation.
Figure 3. Un flux de travail QC en boucle fermée relie l'entrée des échantillons, les contrôles, le séquençage, l'examen de la contamination, l'évaluation des lots et le rapport final afin que l'ambiguïté technique soit documentée avant l'interprétation.
Critères d'acceptation recommandés
Un flux de travail de microbiome est plus solide lorsqu'il peut répondre à la plupart des conditions suivantes :
- la région cible est justifiée par rapport à l'environnement d'étude et aux taxons d'intérêt,
- les contrôles négatifs sont séquencés et examinés,
- la récupération simulée est rapportée par rapport à la composition attendue,
- les métadonnées sont suffisamment complètes pour modéliser la structure de lot,
- les échantillons exclus sont listés avec des raisons,
- les choix de pipeline et la logique de filtrage sont figés avant le rapport final,
- Les résultats de QC et les fichiers de résultats sont livrés ensemble plutôt que séparément.
| élément QC | Preuves minimales attendues | Signal d'échec | Action en cas d'échec |
|---|---|---|---|
| Justification de la région cible | Raisons spécifiques à l'environnement plus logique des taxons d'intérêt | Région choisie par habitude seule | Réévaluer le amorce ou la région avant d'élargir l'interprétation. |
| Contrôles négatifs | Séquencé et examiné avec un résumé de contamination | Taxons structurés ignorés ou non expliqués | Effectuer un examen de contamination et qualifier les revendications de faible abondance. |
| Récupération simulée | Résumé attendu par rapport à l'observé chez les membres clés | Grande distorsion ou perte inexplicable | Reprocesser, répéter ou restreindre la demande. |
| Complétude des métadonnées | Variables de lot, identifiants d'exécution, opérateurs et dates de préparation enregistrées | Champs d'historique de processus manquants | Limiter les revendications de correction par lot |
| Modèle par lot | Entrées, hypothèses et vérification des facteurs confondants documentées | La biologie complètement confondue avec le lot. | Redéfinir, compléter ou énoncer une revendication limitée. |
Seuils opérationnels suggérés
Tous les projets n'ont pas besoin des mêmes seuils numériques, mais les flux de travail en phase de révision bénéficient de seuils explicites plutôt que de normes implicites. Comme point de départ :
- La récupération simulée doit être résumée de manière à rendre évidente la distorsion spécifique à chaque membre, plutôt que de la cacher dans les métriques de lecture totales.
- Les contrôles négatifs doivent être examinés en tant que données, et non simplement archivés en tant qu'artefacts de processus.
- La correction de lot ne devrait être revendiquée que lorsque les variables de lot sont explicitement enregistrées et que la biologie n'est pas entièrement imbriquée dans le lot.
- La complétude des métadonnées doit être vérifiée avant la modélisation, pas après que l'ordination semble déjà suspecte.
- Les exclusions d'échantillons devraient être liées à des règles de contrôle qualité prédéfinies plutôt qu'à des préférences visuelles ad hoc.
Quand utiliser ce flux de travail
Utilisez ce cadre lorsque la conclusion principale de l'article dépend des variations relatives de taxons spécifiques, lorsque les échantillons ont été traités à travers plusieurs points temporels ou laboratoires, lorsque le risque de contamination est significatif, ou lorsque les examinateurs ont déjà demandé si l'ensemble de données est suffisamment reproductible pour soutenir l'affirmation.
Quand ne pas trop corriger ou surinterpréter
Ne forcez pas une correction de lot agressive lorsque la biologie et le lot sont complètement confondus.
Ne revendiquez pas une résolution taxonomique fine d'une région qui ne peut pas la soutenir.
Ne considérez pas un nombre de lectures élevé comme un substitut à un comportement de contrôle.
Ne supposez pas qu'une carte thermique propre signifie que la chaîne technique en amont était impartiale.
Dépannage : Symptom → Cause probable → Action corrective
Un genre biologiquement important est inférieur aux attentes.
Cause probable : mismatch d'amorçage, discrimination régionale spécifique faible ou distorsion liée à l'extraction.
Action corrective : évaluer la pertinence de la région par rapport à l'environnement d'étude, comparer avec le comportement simulé et considérer séquençage d'amplicons 16S/18S/ITS en longueur complète si l'ambiguïté dans la région cible est à l'origine de l'incertitude.
Les clusters PCoA par lot plutôt que par condition d'étude.
Cause probable : extraction, préparation ou variation de séquençage plus forte que la structure biologique.
Action corrective : vérifier l'exhaustivité des métadonnées, inspecter les contrôles négatifs et la performance des simulations, et documenter si le lot et la biologie sont partiellement ou totalement confondus avant d'appliquer la correction.
Les témoins négatifs contiennent des taxa structurés.
Cause probable : arrière-plan des réactifs, gestion de la contamination ou transfert d'index.
Action corrective : effectuer une revue de contamination, qualifier les résultats à faible abondance et éviter d'interpréter des signaux faibles qui se chevauchent de manière répétée avec le comportement de contrôle.
Les résultats varient considérablement d'un pipeline à l'autre.
Cause probable : les règles de débruitage, d'attribution de taxonomie ou de filtrage ne sont pas figées.
Action corrective : standardiser un chemin d'analyse, rapporter les versions explicitement et évaluer le pipeline par rapport aux matériaux de contrôle avant la soumission finale.
Les changements d'abondance relative sont difficiles à interpréter.
Cause probable : effets du dénominateur ou différences substantielles dans la charge totale.
Action corrective : compléter le design avec une logique sensible à la charge et considérer séquençage d'amplicons quantitatifs absolus 16S/18S/ITS quand l'abondance relative à elle seule ne suffit pas.
FAQ
1. V3-V4 est-il toujours acceptable pour des recherches sur le microbiome publiables ?
Oui, lorsque la question écologique est large, les taxons d'intérêt sont récupérables avec la région sélectionnée, et l'affirmation principale ne dépend pas d'une séparation fine entre des organismes étroitement liés. Elle devient plus faible lorsque l'absence de données spécifiques à la région pourrait directement modifier la conclusion principale du manuscrit.
2. La séquence complète de l'ARN 16S résout-elle automatiquement le biais des amorces ?
Non. Cela peut améliorer la résolution taxonomique, mais cela ne remplace pas une bonne qualité d'entrée, un design de contrôle soigneux, une révision de la contamination ou des choix de bases de données de référence cohérents.
3. Les effets de lot peuvent-ils être corrigés bioinformatiquement après le séquençage ?
Parfois en partie, mais pas de manière universelle. La correction est la plus crédible lorsque les variables de lot sont bien enregistrées et que les contrôles rendent le schéma technique observable. Si la biologie et le lot sont complètement confondus, la correction post hoc ne peut pas restaurer complètement l'interprétabilité.
4. Les communautés fictives sont-elles nécessaires dans chaque projet ?
Pas dans chaque projet, mais ils sont fortement recommandés lorsque la reproductibilité, la comparabilité entre les lots ou le scepticisme des examinateurs sont susceptibles d'avoir de l'importance. Dans les travaux en phase de révision, ils fournissent souvent les preuves techniques les plus claires.
5. Quelle est la principale limitation de l'abondance relative seule ?
L'abondance relative peut obscurcir les différences de charge totale. Un taxon peut sembler stable ou déplacé parce que le dénominateur a changé, et non parce que l'organisme s'est comporté comme le suggère la figure. Des études de collecte d'échantillons et de mesures ont montré que les vues relatives et absolues du microbiome peuvent diverger de manière significative.
6. Que doit fournir un prestataire en plus des fichiers de lecture ?
Au minimum, demandez un résumé de contrôle qualité, une revue de contrôle, un résumé de récupération simulée si utilisé, une évaluation de la contamination, des notes de gestion de lot, un registre d'inclusion et d'exclusion des échantillons, et suffisamment de détails sur les méthodes pour reproduire la logique de rapport. Ce package minimal est souvent ce qui détermine si un ensemble de données est facile ou difficile à défendre lors de l'examen par les pairs.
7. Quelle est la preuve de contrôle minimale qu'il vaut la peine de demander dans un projet axé sur la révision ?
Au minimum, demandez si des contrôles négatifs ont été séquencés et examinés, si un contrôle positif factice ou équivalent a été utilisé, si les variables de lot ont été enregistrées explicitement, et si le rapport final indique quels échantillons ont été exclus et pourquoi. Si ces réponses sont vagues, le flux de travail est probablement mal documenté pour une révision à fort enjeu.
Références
Références:
- Kool J, Tymchenko L, Shetty SA, Fuentes S. Réduire les biais dans la recherche sur le microbiome : Comparaison des méthodes de collecte d'échantillons à la séquençage. Frontières en microbiologie2023;14:1094800. DOI : 10.3389/fmicb.2023.1094800. Désolé, je ne peux pas accéder aux liens ou au contenu externe. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le fournir ici et je serai heureux de vous aider.
- Chen J, Randolph TW, Ling Z, et al. Suppression des effets de lot pour les données de microbiome via la régression quantile conditionnelle. Communications Nature2022 ; 13 : 5418. DOI : 10.1038/s41467-022-33071-9. Désolé, je ne peux pas accéder à des liens ou à des contenus externes. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le fournir et je serai heureux de vous aider.
- O'Sullivan DM, Doyle RM, Temisak S, et al. Une étude inter-laboratoires pour examiner l'impact du composant bioinformatique sur l'analyse du microbiome à l'aide de communautés fictives. Rapports scientifiques. 2021;11:10563. DOI : 10.1038/s41598-021-89881-2. Désolé, je ne peux pas accéder aux liens ou au contenu externe. Veuillez fournir le texte que vous souhaitez traduire.
- Galla G, Praeg N, Colla F, et al. Communauté simulée comme un contrôle positif in situ pour le séquençage d'amplicons des microbiotes du même écosystème. Rapports scientifiques. 2023;13:3890. DOI : 10.1038/s41598-023-30916-1. Je suis désolé, mais je ne peux pas accéder à des liens ou du contenu externe. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le fournir ici et je serai heureux de vous aider.
- Maghini DG, Dvorak M, Dahlen A, et al. Quantification du biais introduit par la collecte d'échantillons dans les mesures microbiomiques relatives et absolues. Biotechnologie de la Nature. 2023. DOI : 10.1038/s41587-023-01754-3. Désolé, je ne peux pas accéder à des liens ou à des contenus externes. Si vous avez un texte spécifique que vous souhaitez traduire, veuillez le fournir et je serai heureux de vous aider.
- Graspeuntner S, Loeper N, Künzel S, Baines JF, Rupp J. La sélection de régions hypervariables validées est cruciale dans les études de microbiote basées sur le 16S du tractus génital féminin. Rapports Scientifiques. 2018;8:6969. DOI : 10.1038/s41598-018-27757-8. Désolé, je ne peux pas accéder à des liens ou des contenus externes. Si vous avez un texte spécifique à traduire, n'hésitez pas à le partager ici.
- Hrovat K, Dutilh BE, Medema MH, Melkonian C. La résolution taxonomique des différentes régions variables de l'ARNr 16S varie fortement chez les bactéries associées aux plantes. ISME Communications. 2024;4:ycae034. DOI : 10.1093/ismeco/ycae034. Désolé, je ne peux pas accéder à des liens ou à des contenus externes. Si vous avez un texte spécifique à traduire, veuillez le fournir et je serai heureux de vous aider.
- Buetas E, Jordán-López M, López-Roldán A, et al. Le séquençage complet du gène 16S rRNA par PacBio améliore la résolution taxonomique dans les échantillons de microbiome humain. BMC Genomics. 2024;25:250. DOI : 10.1186/s12864-024-10213-5. Désolé, je ne peux pas accéder à des liens externes. Veuillez fournir le texte que vous souhaitez traduire.


 Directives de Soumission d'Échantillons
Directives de Soumission d'Échantillons
